Il est bien établi que l’exercice physique est bénéfique pour le corps. Une activité régulière ne se contente pas de renforcer les muscles, elle améliore également la santé des os, des vaisseaux sanguins et du système immunitaire.
Les ingénieurs du MIT ont récemment découvert que l’exercice a également des effets positifs sur les neurones individuels. Ils ont observé que la contraction des muscles pendant l’exercice libère une série de signaux biochimiques appelés myokines. Lorsqu’ils sont exposés à ces signaux, les neurones se développent quatre fois plus que ceux qui ne le sont pas. Ces résultats au niveau cellulaire suggèrent que l’exercice peut avoir un impact biochimique significatif sur la croissance nerveuse.
De manière surprenante, les chercheurs ont aussi découvert que les neurones réagissent non seulement aux signaux biochimiques de l’exercice, mais aussi à ses effets physiques. Ils ont constaté que lorsque les neurones sont soumis à des mouvements répétés, similaires aux contractions et dilatations musculaires pendant l’exercice, ils se développent autant que lorsqu’ils sont exposés aux myokines.
Bien que des études antérieures aient suggéré un lien biochimique entre l’activité musculaire et la croissance nerveuse, cette recherche est la première à démontrer que les effets physiques sont tout aussi cruciaux. Les résultats, publiés aujourd’hui dans la revue Advanced Healthcare Materials, mettent en lumière la connexion entre muscles et nerfs durant l’exercice, et pourraient influencer les thérapies basées sur l’exercice pour réparer les nerfs endommagés.
« Maintenant que nous savons que cette interaction muscle-nerf existe, elle pourrait être utile pour traiter des problèmes comme les lésions nerveuses, où la communication entre le nerf et le muscle est interrompue », explique Ritu Raman, professeur adjoint au MIT. « Peut-être qu’en stimulant le muscle, nous pourrions encourager la guérison du nerf et restaurer la mobilité chez ceux qui l’ont perdue à cause d’un traumatisme ou d’une maladie neurodégénérative. »
Raman est l’auteur principal de cette nouvelle étude, à laquelle ont contribué Angel Bu, Ferdows Afghah, Nicolas Castro, Maheera Bawa, Sonika Kohli, Karina Shah, et Brandon Rios du Département de génie mécanique du MIT, ainsi que Vincent Butty du Koch Institute for Integrative Cancer Research du MIT.
Discussion musculaire
En 2023, Raman et ses collègues ont rapporté qu’ils pouvaient restaurer la mobilité chez des souris ayant subi une lésion musculaire traumatique en implantant du tissu musculaire sur le site de la blessure, puis en stimulant ce tissu avec de la lumière. Avec le temps, ils ont découvert que le greffon aidait les souris à retrouver leur fonction motrice, atteignant des niveaux d’activité comparables à ceux des souris saines.
En analysant le greffon, ils ont constaté qu’un exercice régulier stimulait le muscle greffé à produire des signaux biochimiques favorisant la croissance des nerfs et des vaisseaux sanguins.
« C’était intéressant car nous pensons toujours que les nerfs contrôlent les muscles, mais rarement que les muscles répondent aux nerfs », explique Raman. « Nous avons donc commencé à penser que stimuler les muscles encourageait la croissance nerveuse. Cependant, il est difficile de prouver que le nerf se développe davantage à cause du muscle, plutôt que d’autres facteurs comme le système immunitaire. »
Dans leur nouvelle étude, l’équipe a cherché à déterminer si l’exercice musculaire avait un effet direct sur la croissance des nerfs, en se concentrant uniquement sur les tissus musculaires et nerveux. Ils ont transformé des cellules musculaires de souris en fibres longues qui ont fusionné pour former une petite feuille de tissu musculaire mature.
L’équipe a génétiquement modifié le muscle pour qu’il se contracte en réponse à la lumière, permettant de simuler l’exercice. Raman a développé un tapis de gel innovant pour cultiver et exercer le tissu musculaire, empêchant le tissu de se détacher pendant l’exercice.
L’équipe a ensuite collecté des échantillons de la solution environnante, pensant qu’elle contenait des myokines, notamment des facteurs de croissance, de l’ARN et d’autres protéines.
« Je considère les myokines comme une soupe biochimique sécrétée par les muscles, dont certaines pourraient être bénéfiques pour les nerfs », explique Raman. « Les muscles sécrètent presque toujours des myokines, mais l’exercice en augmente la production. »
« L’exercice comme médicament »
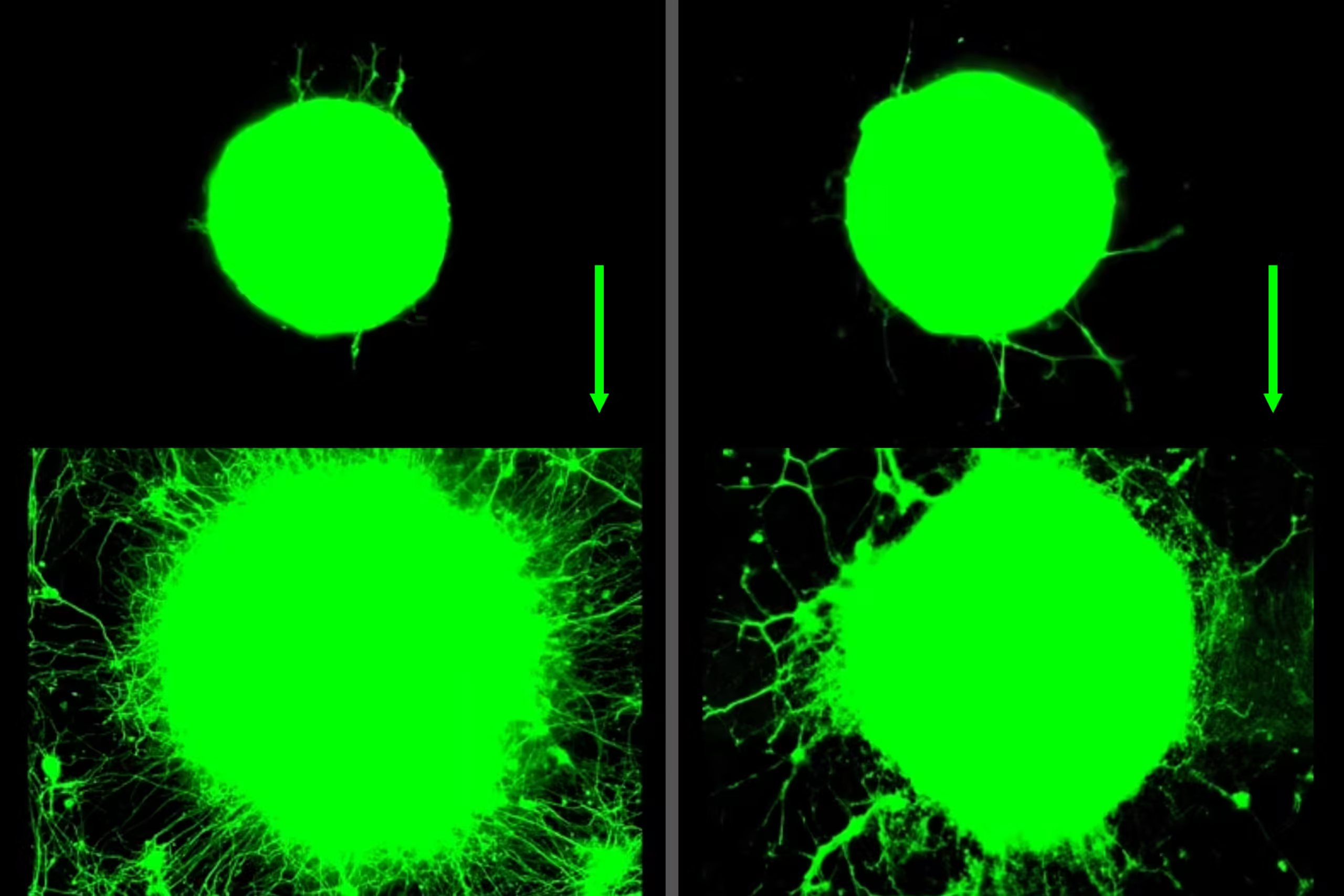
L’équipe a transféré la solution de myokine dans une assiette contenant des motoneurones, des nerfs qui contrôlent les muscles impliqués dans les mouvements volontaires. Les chercheurs ont cultivé ces neurones à partir de cellules souches de souris. Après exposition aux myokines, les neurones ont commencé à se développer rapidement, quatre fois plus vite que ceux non exposés.
« Ils poussent beaucoup plus loin et plus vite, et l’effet est assez immédiat », note Raman.
Pour comprendre comment les neurones changent en réponse aux myokines, l’équipe a effectué une analyse génétique, examinant l’ARN des neurones pour voir si les myokines modifiaient l’expression de certains gènes.
« Nous avons vu que de nombreux gènes régulés positivement dans les neurones stimulés par l’exercice étaient liés à la croissance, à la maturation, et à la communication des neurones », explique Raman. « L’exercice semble influencer non seulement la croissance des neurones, mais aussi leur maturité et leur fonctionnement. »
Les résultats suggèrent que les effets biochimiques de l’exercice favorisent la croissance des neurones. L’équipe s’est alors demandé si les impacts physiques de l’exercice pourraient avoir un bénéfice similaire.
« Les neurones sont physiquement attachés aux muscles, ils s’étirent et bougent donc également avec le muscle », explique Raman. « Nous voulions voir si, même sans signaux biochimiques, étirer les neurones pourrait influencer leur croissance. »
Pour tester cela, les chercheurs ont développé des motoneurones sur un tapis de gel avec de minuscules aimants. Ils ont utilisé un aimant externe pour faire bouger le tapis et les neurones, simulant un exercice mécanique. Ils ont découvert que cet exercice stimulait la croissance des neurones autant que les myokines.
« C’est un bon signe car cela montre que les effets biochimiques et physiques de l’exercice sont tout aussi importants », explique Raman.
Maintenant que le groupe a montré que l’exercice musculaire peut favoriser la croissance nerveuse, ils envisagent d’étudier comment la stimulation musculaire ciblée peut être utilisée pour guérir les nerfs endommagés et restaurer la mobilité chez les personnes atteintes de maladies neurodégénératives comme la SLA.
« Ce n’est que notre premier pas vers la compréhension et le contrôle de l’exercice en tant que médicament », conclut Raman.